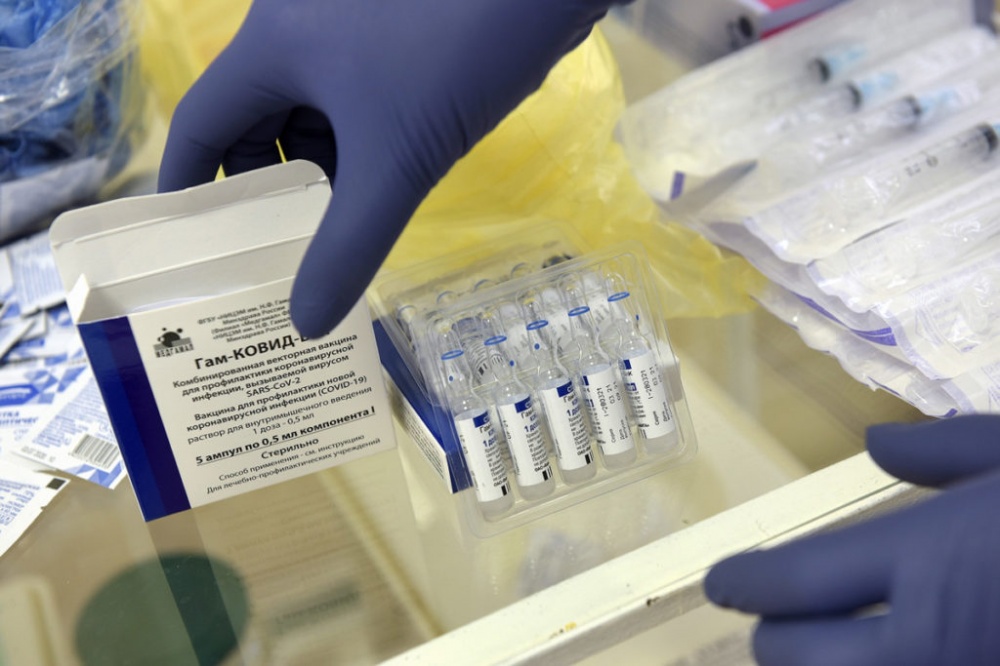
«Производители вакцин должны подтвердить, что места, где производятся вакцины, согласуются со стандартами надлежащих практик производства. Что касается процесса одобрения вакцины «Спутник» для экстренного применения, то он приостановлен, потому что во время инспекции одной из фабрик, где в том числе производится Спутник V, выяснилось несоответствие правилам GMP. <....> Должны быть приняты меры, проведены необходимые изменения и организована новая инспекция. Процесс приостановлен до того, как это произойдет», – заявил Барбоса.
Спутник V производится на мощностях НИЦЭМ им. Н.Ф. Гамалеи, «Биннофарма», «Р-Фарма», «Биокада», «Генериума», ЗАО «Лекко» и «Фармстандарт-УфаВита».
В июне ВОЗ провела инспекцию четырех из семи российских площадок, на которых выпускается Спутник V, по заявке России на одобрение вакцины для экстренного использования в других странах. На уфимском предприятии «Фармстандарта» инспекторы обнаружили нарушения.
В результате инспекции завода «Фармстандарт-УфаВита» ВОЗ выразила опасения по поводу целостности данных и результатов мониторингов – микробиологического и окружающей среды – во время производства и контроля качества вакцины, контроля работы на асептических участках и при розливе вакцин, прослеживаемости и идентификации партий Спутника V и его компонентов, принятия мер по снижению рисков перекрестного загрязнения, обеспечения стерильности на линиях розлива и защиты операторов линий, проблем с проверкой стерильной фильтрации вакцины.
По словам пресс-секретаря президента РФ Дмитрия Пескова, все замечания были приняты во внимание, а недочеты исправлены.
Представители Европейского агентства по лекарственным средствам, как и ВОЗ, проводили инспекцию производственных мощностей вакцины «Спутник V», но от замечаний воздержались.